Щелочноземельные металлы в химии
К щелочноземельным металлам относятся металлы IIA группы Периодической системы Д.И. Менделеева – кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Кроме них в главную подгруппу II группы входят бериллий (Be) и магний (Mg). На внешнем энергетическом уровне щелочноземельных металлов находится два валентных электрона. Электронная конфигурация внешнего энергетического уровня щелочноземельных металлов – ns2. В своих соединениях они проявляют единственную степень окисления равную +2. В ОВР являются восстановителями, т.е. отдают электрон.
С увеличением заряда ядра атомов элементов, входящих в группу щелочноземельных металлов, энергия ионизации атомов уменьшается, а радиусы атомов и ионов увеличиваются, металлические признаки химических элементов усиливаются.
Физические свойства щелочноземельных металлов
В свободном состоянии Be – металл серо-стального цвета, обладающий плотной гексагональной кристаллической решеткой, достаточно твердый и хрупкий. На воздухе Be покрывается оксидной пленкой, что придает ему матовый оттенок и снижает его химическую активность.
Магний в виде простого вещества представляет собой белый металл, который, также, как и Be, при нахождении на воздухе приобретает матовый оттенок за счет образующейся оксидной пленки. Mg мягче и пластичнее бериллия. Кристаллическая решетка Mg – гексагональная.
Ca, Ba и Sr в свободном виде – серебристо-белые металлы. При нахождении на воздухе мгновенно покрываются желтоватой пленкой, которая представляет собой продукты их взаимодействия с составными частями воздуха. Кальций – достаточно твердый металл, Ba и Sr – мягче.
Ca и Sr имею кубическую гранецентрированную кристаллическую решетку, барий – кубическую объемоцентрированную кристаллическую решетку.
Все щелочноземельные металлы характеризуются наличием металлического типа химической связи, что обуславливает их высокую тепло- и электропроводность. Температуры кипения и плавления щелочноземельных металлов выше, чем щелочных металлов.
Получение щелочноземельных металлов
Получение Be осуществляют по реакции восстановления его фторида. Реакция протекает при нагревании:
BeF2 + Mg = Be + MgF2
Магний, кальций и стронций получают электролизом расплавов солей, чаще всего – хлоридов:
CaCl2 = Ca + Cl2↑
Причем, при получении Mg электролизом расплава дихлорида для понижения температуры плавления в реакционную смесь добавляют NaCl.
Для получения Mg в промышленности используют металло- и углетермические методы:
2(CaO×MgO) (доломит) + Si = Ca2SiO4 + Mg
Основной способ получения Ba – восстановление оксида:
3BaO + 2Al = 3Ba + Al2O
Химические свойства щелочноземельных металлов
Поскольку в н.у. поверхность Be и Mg покрыта оксидной пленкой – эти металлы инертны по отношению к воде. Ca, Sr и Ba растворяются в воде с образованием гидроксидов, проявляющих сильные основные свойства:
Ba + H2O = Ba(OH)2 + H2↑
Щелочноземельные металлы способны реагировать с кислородом, причем все они, за исключением бария, в результате этого взаимодействия образуют оксиды, барий – пероксид:
2Ca + O2 = 2CaO
Ba + O2 = BaO2
Оксиды щелочноземельных металлов, за исключением бериллия, проявляют основные свойства, Be – амфотерные свойства.
При нагревании щелочноземельные металлы способны к взаимодействию с неметаллами (галогенами, серой, азотом и др.):
Mg + Br2 =2MgBr
3Sr + N2 = Sr3N2
2Mg + 2C = Mg2C2
Ca +S = CaS
2Ba + 2P = Ba3P2
Ba + H2 = BaH2
Щелочноземельные металлы реагируют с кислотами – растворяются в них:
Ca + 2HCl = CaCl2 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Бериллий реагирует с водными растворами щелочей – растворяется в них:
Be + 2NaOH + 2H2O = Na2[Be(OH)4] + H2↑
Качественные реакции
Качественной реакцией на щелочноземельные металлы является окрашивание пламени их катионами: Ca2+ окрашивает пламя в темно-оранжевый цвет, Sr
Качественной реакцией на катион бария Ba2+ являются анионы SO42-, в результате чего образуется белый осадок сульфата бария (BaSO4), нерастворимый в неорганических кислотах.
Ba2+ + SO42- = BaSO4↓
Примеры решения задач
ru.solverbook.com
Характерные химические свойства Be, Mg и щелочноземельных металлов » HimEge.ru
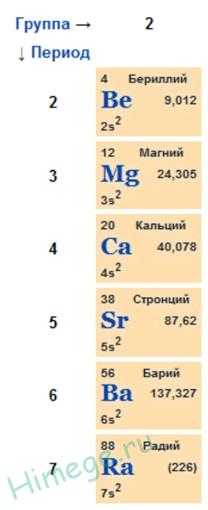 К семейству щёлочноземельных элементов относят кальций, стронций, барий и радий. Д. И. Менделеев включал в это семейство и магний. Щёлочноземельными элементы именуются по той причине, что их гидроксиды, подобно гидроксидам щелочных металлов, растворимы в воде, т. е. являются щелочами. «…Земельными же они названы потому, что в природе они встречаются в состоянии соединений, образующих нерастворимую массу земли, и сами в виде окисей RO имеют землистый вид», — пояснял Менделеев в «Основах химии».
К семейству щёлочноземельных элементов относят кальций, стронций, барий и радий. Д. И. Менделеев включал в это семейство и магний. Щёлочноземельными элементы именуются по той причине, что их гидроксиды, подобно гидроксидам щелочных металлов, растворимы в воде, т. е. являются щелочами. «…Земельными же они названы потому, что в природе они встречаются в состоянии соединений, образующих нерастворимую массу земли, и сами в виде окисей RO имеют землистый вид», — пояснял Менделеев в «Основах химии».Общая характеристика элементов II а группы
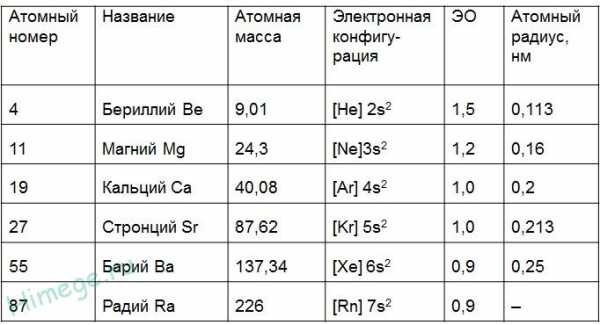
•Металлы главной подгруппы II группы имеют электронную конфигурацию внешнего энергетического уровня ns², и являются s-элементами.
• Легко отдают два валентных электрона, и во всех соединениях имеют степень окисления +2
• Сильные восстановители
•Активность металлов и их восстановительная способность увеличивается в ряду: Be–Mg–Ca–Sr–Ba
• К щёлочноземельным металлам относят только кальций, стронций, барий и радий, реже магний
• Бериллий по большинству свойств ближе к алюминию
Физические свойства простых веществ
Щелочноземельные металлы (по сравнению со щелочными металлами) обладают более высокими t°пл. и t°кип., потенциалами ионизации, плотностями и твердостью.
Химические свойства щелочноземельных металлов + Be
1. Реакция с водой.
В обычных условиях поверхность Be и Mg покрыты инертной оксидной пленкой, поэтому они устойчивы по отношению к воде. В отличие от них Ca, Sr и Ba растворяются в воде с образованием щелочей:
Mg + 2H2O –t°→ Mg(OH)2 + H2↑
Ca + 2H2O → Ca(OH)2 + H2↑
2. Реакция с кислородом.
Все металлы образуют оксиды RO, барий-пероксид – BaO2:
2Mg + O2 → 2MgO
Ba + O2 → BaO2
3. С другими неметаллами образуют бинарные соединения:
Be + Cl2 → BeCl2 (галогениды)
Ba + S → BaS (сульфиды)
3Mg + N2 → Mg3N2 (нитриды)
Ca + H2 → CaH2 (гидриды)
Ca + 2C → CaC2
(карбиды)3Ba + 2P → Ba3P2 (фосфиды)
Бериллий и магний сравнительно медленно реагируют с неметаллами.
4. Все щелочноземельные металлы растворяются в кислотах:
Ca + 2HCl → CaCl2 + H2
Mg + H2SO4(разб.) → MgSO4 + H2
5. Бериллий растворяется в водных растворах щелочей:
Be + 2NaOH + 2H2O → Na2[Be(OH)4] + H2
6. Летучие соединения щёлочноземельных металлов придают пламени характерный цвет:
соединения кальция — кирпично-красный, стронция — карминово-красный, а бария — желтовато-зелёный.
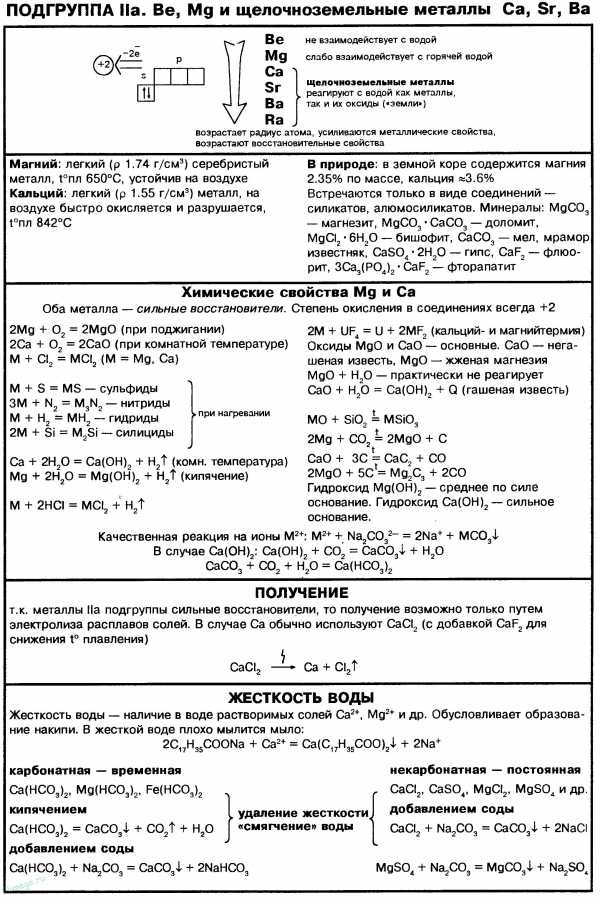
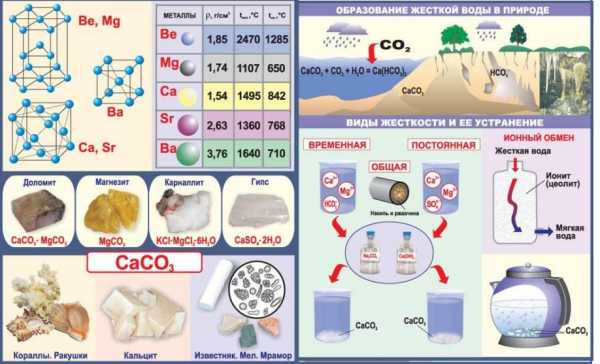 Бериллий, также как и литий, относится к числу s-элементов. Четвертый электрон, появляющийся в атоме Be, помещается на 2s-орбитали. Энергия ионизации бериллия выше, чем у лития, из-за большего заряда ядра. В сильных основаниях он образует ион-бериллат ВеО
Бериллий, также как и литий, относится к числу s-элементов. Четвертый электрон, появляющийся в атоме Be, помещается на 2s-орбитали. Энергия ионизации бериллия выше, чем у лития, из-за большего заряда ядра. В сильных основаниях он образует ион-бериллат ВеО
Высокой энергией ионизации атома бериллий заметно отличается от остальных элементов ПА-подгруппы (магния и щелочноземельных металлов). Его химия во многом сходна с химией алюминия (диагональное сходство). Таким образом, это элемент с наличием у его соединений амфотерных качеств, среди которых преобладают все же основные.
Электронная конфигурация Mg: 1s22s22p63s2 по сравнению с натрием имеет одну существенную особенность: двенадцатый электрон помещается на 2s-орбитали, где уже имеется 1е—.
Ионы магния и кальция ‑ незаменимые элементы жизнедеятельности любой клетки. Их соотношение в организме должно быть строго определённым. Ионы магния участвуют в деятельности ферментов (например, карбоксилазы), кальция – в построении скелета и обмена веществ. Повышение содержания кальция улучшает усвоение пищи. Кальций возбуждает и регулирует работу сердца. Его избыток резко усиливает деятельность сердца. Магний играет отчасти роль антагониста кальция. Введение ионов Mg 2+ под кожу вызывает наркоз без периода возбуждения, паралич мышц, нервов и сердца. Попадая в рану в форме металла, он вызывает долго незаживающие гнойные процессы. Оксид магния в лёгких вызывает так называемую литейную лихорадку. Частый контакт поверхности кожи с его соединениями приводит к дерматитам. Самые широко используемые в медицине соли кальция: сульфат СаSO4 и хлорид CaCL2. Первый используется для гипсовых повязок, а второй применяется для внутривенных вливаний и как внутреннее средство. Он помогает бороться с отёками, воспалениями, аллергией, снимает спазмы сердечно-сосудистой системы, улучшает свертываемость крови.
Все соединения бария, кроме BaSO4, ядовиты. Вызывают менегоэнцефалит с поражением мозжечка, поражение гладких сердечных мышц, паралич, а в больших дозах – дегенеративные изменения печени. В малых же дозах соединения бария стимулируют деятельность костного мозга.
При введении в желудок соединений стронция наступает его расстройство, паралич, рвота; поражения по признакам сходны с поражениями от солей бария, но соли стронция менее токсичны. Особую тревогу вызывает появление в организме радиоактивного изотопа стронция 90Sr. Он исключительно медленно выводится из организма, а его большой период полураспада и, следовательно, длительность действия могут служить причиной лучевой болезни.
Радий опасен для организма своим излучением и огромным периодом полураспада (Т1/2 = 1617 лет). Первоначально после открытия и получения солей радия в более или менее чистом виде его стали использовать довольно широко для рентгеноскопии, лечения опухолей и некоторых тяжёлых заболеваний. Теперь с появлением других более доступных и дешевых материалов применение радия в медицине практически прекратилось. В некоторых случаях его используют для получения радона и как добавку в минеральные удобрения.
В атоме кальция завершается заполнение 4s-орбитали. Вместе с калием он образует пару s-элементов четвертого периода. Гидроксид кальция ‑ довольно сильное основание. У кальция — наименее активного из всех щелочноземельных металлов — характер связи в соединениях ионный.
По своим характеристикам стронций занимает промежуточное положение между кальцием и барием.
Свойства бария наиболее близки к свойствам щелочных металлов.
Бериллий и магний широко используют в сплавах. Бериллиевые бронзы – упругие сплавы меди с 0,5-3% бериллия; в авиационных сплавах (плотность 1,8) содержится 85-90% магния («электрон»). Бериллий отличается от остальных металлов IIА группы – не реагирует с водородом и водой, зато растворяется в щелочах, поскольку образует амфотерный гидроксид:
Be+H2O+2NaOH=Na2[Be(OH)4]+H2.
Магний активно реагирует с азотом:
3 Mg + N2 = Mg3N2 .
В таблице приведена растворимость гидроксидов элементов II группы.
| Растворимость, моль/л (200С) | Растворимость, г/л | |
| Be(OH)2 Mg(OH)2 Ca(OH)2 Sr(OH)2 Ba(OH)2 | 8∙10-6 5∙10-4 2∙10-2 7∙10-2 2∙10-1 | 3,4∙10-4 2,9∙10-2 1,5 8,5 34,2 |
Традиционная техническая проблема – жесткость воды, связанная с наличием в ней ионов Mg2+ и Ca2+ . Из гидрокарбонатов и сульфатов на стенках нагревательных котлов и труб с горячей водой оседают карбонаты магния и кальция и сульфат кальция. Особенно мешают они работе лабораторных дистилляторов.
S-элементы в живом организме выполняют важную биологическую функцию. В таблице приведено их содержание.
Содержание S-элементов в организме человека
| Элемент | Содержание, % |
| Li Na K Rb Cs Be Mg Ca Sr Ba | 10-4 0,08 0,23 10-5 10-4 10-7 0,027 1,4 10-3 10-5 |
Во внеклеточной жидкости содержится в 5 раз больше ионов натрия, чем внутри клеток. Изотонический раствор («физиологическая жидкость») содержит 0,9% хлорида натрия, его применяют для инъекций, промывания ран и глаз и т. п. Гипертонические растворы (3-10% хлорида натрия) используют как примочки при лечении гнойных ран («вытягивание» гноя). 98% ионов калия в организме находится внутри клеток и только 2% во внеклеточной жидкости. В день человеку нужно 2,5-5 г калия. В 100 г кураги содержится до 2 г калия. В 100 г жареной картошки – до 0,5 г калия. Во внутриклеточных ферментативных реакциях АТФ и АДФ участвуют в виде магниевых комплексов.
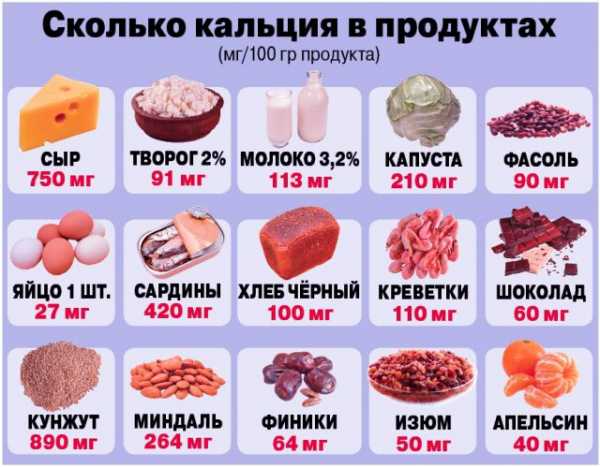
Ежедневно человеку требуется 300-400 мг магния. Он попадает в организм с хлебом (90 мг магния на 100 г хлеба), крупой (в 100 г овсяной крупы до 115 мг магния), орехами (до 230 мг магния на 100 г орехов). Кроме построения костей и зубов на основе гидроксилапатита Ca10(PO4)6(OH)2 , катионы кальция активно участвуют в свертывании крови, передаче нервных импульсов, сокращении мышц. В сутки взрослому человеку нужно потреблять около 1 г кальция. В 100 г твердых сыров содержится 750 мг кальция; в 100 г молока – 120 мг кальция; в 100 г капусты – до 50 мг.
himege.ru
ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ
Свойства щелочноземельных металлов
Физические свойства
Щелочноземельные металлы (по сравнению со щелочными металлами) обладают более высокими t╟пл. и t╟кип., потенциалами ионизации, плотностями и твердостью.
Химические свойства
1. Очень реакционноспособны.
2. Обладают положительной валентностью +2.
3. Реагируют с водой при комнатной температуре (кроме Be) с выделением водорода.
4. Обладают большим сродством к кислороду (восстановители).
5. С водородом образуют солеобразные гидриды ЭH2.
6. Оксиды имеют общую формулу ЭО. Тенденция к образованию пероксидов выражена слабее, чем для щелочных металлов.
Нахождение в природе
Be
3BeO ∙ Al2O3 ∙ 6SiO2 берилл
Mg
MgCO3 магнезит
CaCO3 ∙ MgCO3 доломит
KCl ∙ MgSO4 ∙ 3H2O каинит
KCl ∙ MgCl2 ∙ 6H2O карналлит
Ca
CaCO3 кальцит (известняк, мрамор и др.)
Ca3(PO4)2 апатит, фосфорит
CaSO4 ∙ 2H2O гипс
CaSO4 ангидрит
CaF2 плавиковый шпат (флюорит)
Sr
SrSO4 целестин
SrCO3 стронцианит
Ba
BaSO4 барит
BaCO3 витерит
Получение
Бериллий получают восстановлением фторида:
BeF2 + Mg═ t═ Be + MgF2
Барий получают восстановлением оксида:
3BaO + 2Al═ t═ 3Ba + Al2O3
Остальные металлы получают электролизом расплавов хлоридов:
CaCl2 = Ca + Cl2╜
катод: Ca2+ + 2ē = Ca0
анод: 2Cl— — 2ē = Cl02
MgO + C = Mg + CO
Металлы главной подгруппы II группы — сильные восстановители; в соединениях проявляют только степень окисления +2. Активность металлов и их восстановительная способность увеличивается в ряду: Be Mg Ca Sr Ba╝
1. Реакция с водой.
В обычных условиях поверхность Be и Mg покрыты инертной оксидной пленкой, поэтому они устойчивы по отношению к воде. В отличие от них Ca, Sr и Ba растворяются в воде с образованием гидроксидов, которые являются сильными основаниями:
Mg + 2H2O═ t═ Mg(OH)2 + H2
Ca + 2H2O = Ca(OH)2 + H2╜
2. Реакция с кислородом.
Все металлы образуют оксиды RO, барий-пероксид BaO2:
2Mg + O2 = 2MgO
Ba + O2 = BaO2
3. С другими неметаллами образуются бинарные соединения:
Be + Cl2 = BeCl2 (галогениды)
Ba + S = BaS (сульфиды)
3Mg + N2 = Mg3N2 (нитриды)
Ca + H2 = CaH2(гидриды)
Ca + 2C = CaC2(карбиды)
3Ba + 2P = Ba3P2(фосфиды)
Бериллий и магний сравнительно медленно реагируют с неметаллами.
4. Все металлы растворяются в кислотах:
Ca + 2HCl = CaCl2 + H2╜
Mg + H2SO4(разб.) = MgSO4 + H2╜
Бериллий также растворяется в водных растворах щелочей:
Be + 2NaOH + 2H2O = Na2[Be(OH)4] + H2╜
5. Качественная реакция на катионы щелочноземельных металлов — окрашивание пламени в следующие цвета:
Ca2+ — темно-оранжевый
Sr2+— темно-красный
Ba2+ — светло-зеленый
Катион Ba2+ обычно открывают обменной реакцией с серной кислотой или ее солями:
Сульфат бария — белый осадок, нерастворимый в минеральных кислотах.
Оксиды щелочноземельных металлов
Получение
1) Окисление металлов (кроме Ba, который образует пероксид)
2) Термическое разложение нитратов или карбонатов
CaCO3═ t═ CaO + CO2╜
2Mg(NO3)2═ t═ 2MgO + 4NO2╜ + O2╜
Химические свойства
Типичные основные оксиды. Реагируют с водой (кроме BeO), кислотными оксидами и кислотами
MgO + H2O = Mg(OH)2
3CaO + P2O5 = Ca3(PO4)2
BeO + 2HNO3 = Be(NO3)2 + H2O
BeO — амфотерный оксид, растворяется в щелочах:
BeO + 2NaOH + H2O = Na2[Be(OH)4]
Гидроксиды щелочноземельных металлов R(OH)2
Получение
Реакции щелочноземельных металлов или их оксидов с водой: Ba + 2H2O = Ba(OH)2 + H2
CaO(негашеная известь) + H2O = Ca(OH)2(гашеная известь)
Химические свойства
Гидроксиды R(OH)2 — белые кристаллические вещества, в воде растворимы хуже, чем гидроксиды щелочных металлов (растворимость гидроксидов уменьшается с уменьшением порядкового номера; Be(OH)2 — нерастворим в воде, растворяется в щелочах). Основность R(OH)2 увеличивается с увеличением атомного номера:
Be(OH)2 — амфотерный гидроксид
Mg(OH)2 — слабое основание
остальные гидроксиды — сильные основания (щелочи).
1) Реакции с кислотными оксидами:
Ca(OH)2 + SO2 = CaSO3¯ + H2O
Ba(OH)2 + CO2 = BaCO3¯ + H2O
2) Реакции с кислотами:
Mg(OH)2 + 2CH3COOH = (CH3COO)2Mg + 2H2O
Ba(OH)2 + 2HNO3 = Ba(NO3)2 + 2H2O
3) Реакции обмена с солями:
Ba(OH)2 + K2SO4 = BaSO4¯+ 2KOH
4) Реакция гидроксида бериллия со щелочами:
Be(OH)2 + 2NaOH = Na2[Be(OH)4]
Жесткость воды
Природная вода, содержащая ионы Ca2+ и Mg2+, называется жесткой. Жесткая вода при кипячении образует накипь, в ней не развариваются пищевые продукты; моющие средства не дают пены.
Карбонатная (временная) жесткость обусловлена присутствием в воде гидрокарбонатов кальция и магния, некарбонатная (постоянная) жесткость — хлоридов и сульфатов.
Общая жесткость воды рассматривается как сумма карбонатной и некарбонатной.
Удаление жесткости воды осуществляется путем осаждения из раствора ионов Ca2+ и Mg2+:
1) кипячением:
Сa(HCO3)2═ t═ CaCO3¯ + CO2 + H2O
Mg(HCO3)2═ t═ MgCO3¯ + CO2 + H2O
2) добавлением известкового молока:
Ca(HCO3)2 + Ca(OH)2 = 2CaCO3¯ + 2H2O
3) добавлением соды:
Ca(HCO3)2 + Na2CO3 = CaCO3¯+ 2NaHCO3
CaSO4 + Na2CO3 = CaCO3¯ + Na2SO4
MgCl2 + Na2CO3 = MgCO3¯ + 2NaCl
Для удаления временной жесткости используют все четыре способа, а для постоянной — только два последних.
Термическое разложение нитратов.
Э(NO3)2 =t= ЭO + 2NO2 + 1/2O2
Особенности химиии берилия.
Be(OH)2 + 2NaOH (изб) = Na2[Be(OH)4]
Al(OH)3 + 3NaOH (изб) = Na3[Al(OH)6]
Be + 2NaOH + 2h3O = Na2[Be(OH)4] + h3
Al + 3NaOH + 3h3O = Na3[Be(OH)4] + 3/2h3
Be, Al + HNO3 (Конц) = пассивация
studfiles.net
Щелочноземельные металлы
К понятию щелочноземельных металлов относится часть элементов II группы системы Менделеева: бериллий, магний, кальций, стронций, барий, радий. Четыре последних металла имеют наиболее ярко выраженные признаки щелочноземельной классификации, поэтому в некоторых источниках бериллий и магний не включают в список, ограничиваясь четырьмя элементами.
Свое название металла получили благодаря тому, что при взаимодействии их оксидов с водой образуется щелочная среда. Физические свойства щелочноземельных металлов: все элементы имеют серый металлический цвет, при нормальных условиях имеют твердую структуру, с ростом порядкового номера увеличивается их плотность, имеют очень высокую температуру плавления. В отличие от щелочных металлов, элементы данной группы не режутся ножом (за исключением стронция). Химические свойства щелочноземельных металлов: имеют два валентных электрона, активность растет с повышением порядкового номера, в реакциях выступают в качестве восстановителя.

Характеристика щелочноземельных металлов свидетельствует об их высокой активности. В особенности это относится к элементам с большим порядковым номером. Например, бериллий в нормальных условиях не ступает во взаимодействие с кислородом и галогенами. Для запуска механизма реагирования его необходимо нагреть до температуры свыше 600 градусов по Цельсию. Магний в нормальных условиях имеет на поверхности оксидную пленку и также не реагирует с кислородом. Кальций окисляется, но достаточно медленно. А вот стронций, барий и радий окисляются практически мгновенно, поэтому их хранят в безкислородной среде под керосиновым слоем.
Все оксиды усиливают основные свойства с ростом порядкового номера металла. Гидроксид бериллия представляет собой амфотерное соединение, которое не реагирует с водой, но хорошо растворяется в кислотах. Гидроксид магния является слабой щелочью, нерастворимой в воде, но реагирующей с сильными кислотами. Гидроксид кальция — сильное, малорастворимое в воде основание, реагирующее с кислотами. Гидроксиды бария и стронция относятся к сильным основаниям, хорошо растворимым в воде. А гидроксид радия — это одна из сильнейших щелочей, которая хорошо реагирует с водой и практически всеми видами кислот.
Способы получения
Получают гидроксиды щелочноземельных металлов путем воздействия воды на чистый элемент. Реакция протекает при комнатных условиях (кроме бериллия, для которого требуется повышение температуры) с выделением водорода. При нагревании все щелочноземельные металлы реагируют с галогенами. Полученные соединения используются в производстве большого ассортимента продукции от химических удобрений до сверхточных деталей микропроцессора. Соединения щелочноземельных металлов проявляют такую же высокую активность, как и чистые элементы, поэтому их используют во многих химических реакциях.

Чаще всего это происходит при реакциях обмена, когда необходимо вытеснить из вещества менее активный металл. В окислительно-восстановительных реакциях принимают участие в качестве сильного восстановителя. Двухвалентные катионы кальция и магния придает воде так называемую жесткость. Преодоление этого явления происходит путем осаждения ионов при помощи физического воздействия или добавления в воду специальных смягчающих веществ. Соли щелочноземельных металлов образуются путем растворения элементов в кислоте либо в результате реакций обмена. Полученные соединения имеют прочную ковалентную связь, поэтому обладают невысокой электропроводностью.
В природе щелочноземельные металлы не могут находиться в чистом виде, так как быстро вступают во взаимодействие с окружающей средой, образую химические соединения. Они входят в состав минералов и горных пород, содержащихся в толще земной коры. Наиболее распространен кальций, немного уступает ему магний, довольно часто встречаются барий и стронций. Бериллий относится к редким металлам, а радий — к очень редким. За все время, которое прошло с момента открытия радия, во всем мире было добыто всего полтора килограмма чистого металла. Как и большинство радиоактивных элементов, радий имеет изотопы, коих у него насчитывается четыре штуки.

Получают щелочноземельные металлы путем разложения сложных веществ и выделения из них чистого вещества. Бериллий добывают путем восстановления его из фторида при воздействии высокой температуры. Барий восстанавливает из его оксида. Кальций, магний и стронций получают путем электролиза их хлоридного расплава. Сложнее всего синтезировать чистый радий. Его добывают путем воздействия на урановую руду. По подсчетам ученых в среднем на одну тонну руды приходится 3 грамма чистого радия, хотя встречаются и богатые месторождения, в которых содержится целых 25 грамм на тонну. Для выделения металла используются методы осаждения, дробной кристаллизации и ионного обмена.
Применение щелочноземельных металлов
Спектр применения щелочноземельных металлов очень обширен и охватывает многие отрасли. Бериллий в большинстве случаев используется в качестве легирующей добавки в различные сплавы. Он повышает твердость и прочность материалов, хорошо защищает поверхность от воздействия коррозии. Также благодаря слабому поглощению радиоактивного излучения бериллий используется при изготовлении рентгеновских аппаратов и в ядерной энергетике.
Магний используют как один из восстановителей при получении титана. Его сплавы отличаются высокой прочностью и легкостью, поэтому используются при производстве самолетов, автомобилей, ракет. Оксид магния горит ярким ослепительным пламенем, что нашло отражение в военном деле, где он используется для изготовления зажигательных и трассирующих снарядов, сигнальных ракет и светошумовых гранат. Является одним из важнейших элементов для регуляции нормального процесса жизнедеятельности организма, поэтому входит в состав некоторых лекарств.

Кальций в чистом виде практически не применяют. Он нужен для восстановления других металлов из их соединений, а также в производстве препаратов для укрепления костной ткани. Стронций используют для восстановления других металлов и в качестве основного компонента для производства сверхпроводящих материалов. Барий добавляют во многие сплавы, которые предназначены для работы в агрессивной среде, так как он обладает отличными защитными свойствами. Радий используется в медицине для кратковременного облучения кожи при лечении злокачественных образований.
promplace.ru
Химия щелочноземельных металлы | CHEMEGE.RU
Элементы II группы главной подгруппы
1. Положение в Периодической системе химических элементов
2. Электронное строение и закономерности изменения свойств
3. Физические свойства
4. Нахождение в природе
5. Способы получения
6. Качественные реакции
7. Химические свойства
7.1. Взаимодействие с простыми веществами
7.1.1. Взаимодействие с галогенами
7.1.2. Взаимодействие с серой и фосфором
7.1.3. Взаимодействие с водородом
7.1.4. Взаимодействие с азотом
7.1.5. Взаимодействие с углеродом
7.1.6. Горение
7.2. Взаимодействие со сложными веществами
7.2.1. Взаимодействие с водой
7.2.2. Взаимодействие с минеральными кислотами
7.2.3. Взаимодействие с серной кислотой
7.2.4. Взаимодействие с азотной кислотой
7.2.5. Взаимодействие с оксидами неметаллов
7.2.6. Взаимодействие с солями и оксидами металлов
Оксиды щелочноземельных металлов
1. Способы получения
2. Химические свойства
2.1. Взаимодействие с кислотными и амфотерными оксидами
2.2. Взаимодействие с кислотами
2.3. Взаимодействие с водой
2.4. Амфотерные свойства оксида бериллия
Гидроксиды щелочноземельных металлов
1. Способы получения
2. Химические свойства
2.1. Взаимодействие с кислотами
2.2. Взаимодействие с кислотными оксидами
2.3. Взаимодействие с амфотерными оксидами и гидроксидами
2.4. Взаимодействие с кислыми солями
2.5. Взаимодействие с неметаллами
2.6. Взаимодействие с металлами
2.7. Взаимодействие с солями
2.8. Разложение при нагревании
2.9. Диссоциация
2.10. Амфотерные свойства гидроскида бериллия
Соли щелочноземельных металлов
Жесткость
1. Постоянная и временная жесткость
2. Способы устранения жесткости
Элементы II группы главной подгруппы
Положение в периодической системе химических элементов
Щелочноземельные металлы расположены во второй группе главной подгруппе периодической системы химических элементов Д.И. Менделеева (или просто во 2 группе в длиннопериодной форме ПСХЭ). На практике к щелочноземельным металлам относят только кальций Ca, стронций Sr, барий Ba и радий Ra. Бериллий Be по свойствам больше похож на алюминий, магний Mg проявляет некоторые свойства щелочноземельных металлов, но в целом отличается от них. Однако, согласно номенклатуре ИЮПАК, щелочноземельными принято считать все металлы II группы главной подгруппы.
Электронное строение и закономерности изменения свойств
Электронная конфигурация внешнего энергетического уровня щелочноземельных металлов: ns2, на внешнем энергетическом уровне в основном состоянии находится 2 s-электрона. Следовательно, типичная степень окисления щелочноземельных металлов в соединениях +2.
Рассмотрим некоторые закономерности изменения свойств щелочноземельных металлов.
В ряду Be—Mg—Ca—Sr—Ba—Ra, в соответствии с Периодическим законом, увеличивается атомный радиус, усиливаются металлические свойства, ослабевают неметаллические свойства, уменьшается электроотрицательность.
Физические свойства
Все щелочноземельные металлы — вещества серого цвета и гораздо более твердые, чем щелочные металлы.
Бериллий Be устойчив на воздухе. Магний и кальций (Mg и Ca) устойчивы в сухом воздухе. Стронций Sr и барий Ba хранят под слоем керосина.
Кристаллическая решетка щелочноземельных металлов в твёрдом состоянии — металлическая. Следовательно, они обладают высокой тепло- и электропроводимостью. Кипят и плавятся при высоких температурах.
Нахождение в природе
Как правило, щелочноземельные металлы в природе присутствуют в виде минеральных солей: хлоридов, бромидов, йодидов, карбонатов, нитратов и др. Основные минералы, в которых присутствуют щелочноземельные металлы:
Доломит — CaCO3 · MgCO3 — карбонат кальция-магния.
Магнезит MgCO3 – карбонат магния.
Кальцит CaCO3 – карбонат кальция.
Гипс CaSO4 · 2H2O – дигидрат сульфата кальция.
Барит BaSO4 — сульфат бария.
Витерит BaCO3 – карбонат бария.
Способы получения
Магний получают электролизом расплавленного карналлита или хлорида магния с добавками хлорида натрия при 720–750°С:
MgCl2 → Mg + Cl2
или восстановлением прокаленного доломита в электропечах при 1200–1300°С:
2(CaO · MgO) + Si → 2Mg + Ca2SiO4
Кальций получают электролизом расплавленного хлорида кальция с добавками фторида кальция:
CaCl2 → Ca + Cl2
Барий получают восстановлением оксида бария алюминием в вакууме при 1200 °C:
4BaO+ 2Al → 3Ba + Ba(AlO2)2
Качественные реакции
Качественная реакция на щелочноземельные металлы — окрашивание пламени солями щелочноземельных металлов.
Цвет пламени:
Ca — кирпично-красный
Sr — карминово-красный (алый)
Ba — яблочно-зеленый
Качественная реакция на ионы магния: взаимодействие с щелочами. Ионы магния осаждаются щелочами с образованием белого осадка гидроксида магния:
Mg2+ + 2OH— → Mg(OH)2↓
Качественная реакция на ионы кальция, стронция, бария: взаимодействие с карбонатами. При взаимодействии солей кальция, стронция и бария с карбонатами выпадает белый осадок карбоната кальция, стронция или бария:
Ca2+ + CO32- → CaCO3↓
Ba2+ + CO32- → BaCO3↓
Качественная реакция на ионы стронция и бария: взаимодействие с карбонатами. При взаимодействии солей стронция и бария с сульфатами выпадает белый осадок сульфата бария и сульфата стронция:
Ba2+ + SO42- → BaSO4↓
Sr2+ + SO42- → SrSO4↓
Также осадки белого цвета образуются при взаимодействии солей кальция, стронция и бария с сульфитами и фосфатами.
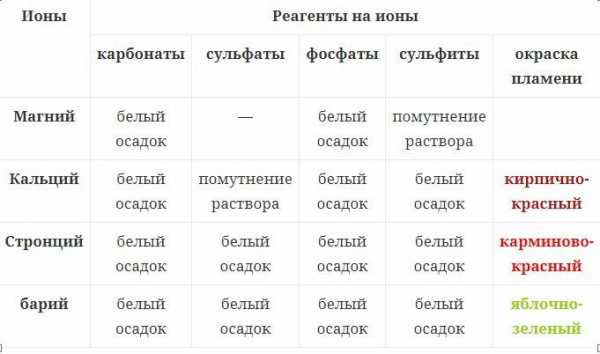
Например, при взаимодействии хлорида кальция с фосфатом натрия образуется белый осадок фосфата кальция:
3CaCl2 + 2Na3PO4 → 6NaCl + 2Ca3(PO4)2↓
Химические свойства
1. Щелочноземельные металлы — сильные восстановители. Поэтому они реагируют почти со всеми неметаллами.
1.1. Щелочноземельные металлы реагируют с галогенами с образованием галогенидов при нагревании.
Например, бериллий взаимодействует с хлором с образованием хлорида бериллия:
Be + Cl2 → BeCl2
1.2. Щелочноземельные металлы реагируют при нагревании с серой и фосфором с образованием сульфидов и фосфоридов.
Например, кальций взаимодействует с серой при нагревании:
Ca + S → CaS
Кальций взаимодействует с фосфором с образованием фосфидов:
3Ca + 2P → Ca3P2
1.3. Щелочноземельные металлы реагируют с водородом при нагревании. При этом образуются бинарные соединения — гидриды. Бериллий с водородом не взаимодействует, магний реагирует лишь при повышенном давлении.
Mg + H2 → MgH2
1.4. С азотом магний взаимодействует при комнатной температуре с образованием нитрида:
6Mg + 2N2 → 2Mg3N2
Остальные щелочноземельные металлы реагируют с азотом при нагревании.
1.5. Щелочноземельные металлы реагируют с углеродом с образованием карбидов, преимущественно ацетиленидов.
Например, кальций взаимодействует с углеродом с образованием карбида кальция:
Ca + 2C → CaC2
Бериллий реагирует с углеродом при нагревании с образованием карбида — метанида:
2Be + C → Be2C
1.6. Бериллий сгорает на воздухе при температуре около 900°С:
2Be + O2 → 2BeO
Магний горит на воздухе при 650°С с выделением большого количества света. При этом образуются оксиды и нитриды:
2Mg + O2 → 2MgO
3Mg + N2 → Mg3N2
Щелочноземельные металлы горят на воздухе при температуре около 500°С, в результате также образуются оксиды и нитриды.
Видеоопыт: горение кальция на воздухе можно посмотреть здесь.
2. Щелочноземельные металлы взаимодействуют со сложными веществами:
2.1. Щелочноземельные металлы реагируют с водой. Взаимодействие с водой приводит к образованию щелочи и водорода. Бериллий с водой не реагирует. Магний реагирует с водой при кипячении. Кальций, стронций и барий реагируют с водой при комнатной температуре.
Например, кальций реагирует с водой с образованием гидроксида кальция и водорода:
2Ca0 + 2H2+O = 2Ca+(OH)2 + H20
2.2. Щелочноземельные металлы взаимодействуют с минеральными кислотами (с соляной, фосфорной, разбавленной серной кислотой и др.). При этом образуются соль и водород.
Например, магний реагирует с соляной кислотой:
2Mg + 2HCl → MgCl2 + H2↑
2.3. При взаимодействии щелочноземельных металлов с концентрированной серной кислотой образуется сера.
Например, при взаимодействии кальция с концентрированной серной кислотой образуется сульфат кальция, сера и вода:
4Ca + 5H2SO4(конц.) → 4CaSO4 + S + 5H2O
2.4. Щелочноземельные металлы реагируют с азотной кислотой. При взаимодействии кальция и магния с концентрированной или разбавленной азотной кислотой образуется оксид азота (I):
4Ca + 10HNO3 (конц) → N2O + 4Сa(NO3)2 + 5H2O
При взаимодействии щелочноземельны металлов с очень разбавленной азотной кислотой образуется нитрат аммония:
4Ba + 10HNO3 → 4Ba(NO3)2 + NH4NO3 + 3H2O
2.5. Щелочноземельные металлы могут восстанавливать некоторые неметаллы (кремний, бор, углерод) из оксидов.
Например, при взаимодействии кальция с оксидом кремния (IV) образуются кремний и оксид кальция:
2Ca + SiO2 → 2CaO + Si
Магний горит в атмосфере углекислого газа. При этом образуется сажа и оксид магния:
2Mg + CO2 → 2MgO + C
2.6. В расплаве щелочноземельные металлы могут вытеснять менее активные металлы из солей и оксидов. Обратите внимание! В растворе щелочноземельные металлы будут взаимодействовать с водой, а не с солями других металлов.
Например, кальций вытесняет медь из расплава хлорида меди (II):
Ca + CuCl2 → CaCl2 + Cu
Оксиды щелочноземельных металлов
Способы получения
1. Оксиды щелочноземельных металлов можно получить из простых веществ — окислением металлов кислородом:
2Ca + O2 → 2CaO
2. Оксиды щелочноземельных металлов можно получить термическим разложением некоторых кислородсодержащих солей — карбонатов, нитратов.
Например, карбонат кальция разлагается на оксид кальция, оксид азота (IV) и кислород:
2Ca(NO3)2 → 2CaO + 4NO2 + O2
MgCO3 → MgO + CO2
СаСО3 → СаО + СО2
3. Оксиды магния и бериллия можно получить термическим разложением гидроксидов:
Mg(OH)2 → MgO + H2O
Химические свойства
Оксиды кальция, стронция, бария и магния — типичные основные оксиды. Вступают в реакции с кислотными и амфотерными оксидами, кислотами, водой. Оксид бериллия — амфотерный.
1. Оксиды кальция, стронция, бария и магния взаимодействуют с кислотными и амфотерными оксидами:
Например, оксид магния взаимодействует с углекислым газом с образованием карбоната магния:
MgO + CO2 → MgCO3
2. Оксиды щелочноземельных металлов взаимодействуют с кислотами с образованием средних и кислых солей (с многоосновными кислотами).
Например, оксид кальция взаимодействует с соляной кислотой с образованием хлорида кальция и воды:
CaO + 2HCl → CaCl2 + H2O
3. Оксиды кальция, стронция и бария активно взаимодействуют с водой с образованием щелочей.
Например, оксид кальция взаимодействует с водой с образованием гидроксида лития:
Li2O + H2O → 2LiOH
Оксид магния реагирует с водой при нагревании:
MgO + H2O → Mg(OH)2
Оксид бериллия не взаимодействует с водой.
4. Оксид бериллия взаимодействует с щелочами и основными оксидами.
При взаимодействии оксида бериллия с щелочами в расплаве или с основными оксидами образуются соли-бериллаты.
Например, оксид натрия реагирует с оксидом бериллия с образованием бериллата натрия:
Na2O + BeO → Na2BeO2
Например, гидроксид натрия реагирует с оксидом бериллия в расплаве с образованием бериллата натрия:
2NaOH + BeO → Na2BeO2 + H2O
При взаимодействии оксида бериллия с щелочами в растворе образуются комплексные соли.
Например, оксид бериллия реагирует с гидроксидом калия с растворе с образованием тетрагидроксобериллата калия:
2NaOH + BeO + H2O → Na2[Be(OH)4]
Гидроксиды щелочноземельных металлов
Способы получения
1. Гидроксиды кальция, стронция и бария получают при взаимодействии соответствующих оксидов с водой.
Например, оксид кальция (негашеная известь) при взаимодействии с водой образует гидроксид кальция (гашеная известь):
CaO + H2O → Ca(OH)2
Оксид магния взаимодействует с водой только при нагревании:
MgO + H2O → Mg(OH)2
2. Гидроксиды кальция, стронция и бария получают при взаимодействии соответствующих металлов с водой.
Например, кальций реагирует с водой с образованием гидроксида кальция и водорода:
2Ca + 2H2O → 2Ca(OH)2 + H2
Магний взаимодействует с водой только при кипячении:
2Mg + 2H2O → 2Mg(OH)2 + H2
3. Гидроксиды кальция и магния можно получить при взаимодействии солей кальция и магния с щелочами.
Например, нитрат кальция с гидроксидом калия образует нитрат калия и гидроксид кальция:
Ca(NO3)2 + 2KOH → Ca(OH)2↓ + 2KNO3
Химические свойства
1. Гидроксиды кальция, стронция и бария реагируют с всеми кислотами (и сильными, и слабыми). При этом образуются средние или кислые соли, в зависимости от соотношения реагентов.
Гидроксид магния взаимодействует только с сильными кислотами.
Например, гидроксид кальция с соляной кислотой реагирует с образова-нием хлорида кальция:
Ca(OH)2 + 2HCl → CaCl2 + 2H2O
2. Гидроксиды щелочных металлов реагируют с кислотными оксидами. При этом образуются средние или кислые соли, в зависимости от соотношения реагентов.
Например, гидроксид бария с углекислым газом реагирует с образова-нием карбонатов или гидрокарбонатов:
Ba(OH)2(избыток) + CO2 → BaCO3 + H2O
Ba(OH)2 + 2CO2(избыток) → Ba(HCO3)2
3. Гидроксиды кальция, стронция и бария реагируют с амфотерными оксидами и гидроксидами. При этом в расплаве образуются средние соли, а в растворе комплексные соли.
Например, гидроксид бария с оксидом алюминия реагирует в расплаве с образованием алюминатов:
Ba(OH)2 + Al2O3 → Ba(AlO2)2 + H2O
в растворе образуется комплексная соль — тетрагидроксоалюминат:
Ba(OH)2 + Al2O3 + 3H2O → Ba[Al(OH)4]2
4. Гидроксиды кальция, стронция и бария взаимодействуют с кислыми солями. При этом образуются средние соли, или менее кислые соли.
Например: гидроксид кальция реагирует с гидрокарбонатом кальция с образованием карбоната кальция:
Ca(OH)2 + Ca(HCO3)2 → 2CaCO3 + 2H2O
5. Гидроксиды кальция, стронция и бария взаимодействуют с простыми веществами-неметаллами (кроме инертных газов, азота, кислорода, водорода и углерода). Взаимодействие щелочей с неметаллами подробно рассмотрено в статье про щелочные металлы.
6. Гидроксиды кальция, стронция и бария взаимодействуют с амфотерными металлами, кроме железа и хрома. При этом в расплаве образуются соль и водород:
Ca(OH)2 + Zn → CaZnO2 + H2
В растворе образуются комплексная соль и водород:
Ca(OH)2 + 2Al + 6Н2О = Ca[Al(OH)4]2 + 3Н2
7. Гидроксиды кальция, стронция и бария вступают в обменные реакции с растворимыми солями. Как правило, с этими гидроксидами реагируют растворимые соли тяжелых металлов (в ряду активности расположены правее алюминия), а также растоворимые карбонаты, сульфиты, силикаты, и, для гидроксидов стронция и бария — растворимые сульфаты.
Например, хлорид железа (II) реагирует с гидроксидом бария с образованием хлорида бария и осадка гидроксида железа (II):
Ba(OH)2 + FeCl2 = BaCl2+ Fe(OH)2↓
Также с гидроксидами кальция, стронция и бария взаимодействуют соли аммония.
Например, при взаимодействии бромида аммония и гидроксида кальция образуются бромид кальция, аммиак и вода:
2NH4Cl + Ca(OH)2 = 2NH3 + 2H2O + CaCl2
8. Гидроксид кальция разлагается при нагревании до 580оС, гидроксиды магния и бериллия разлагаются при нагревании:
Mg(OH)2 → MgO + H2O
9. Гидроксиды кальция, стронция и бария проявляют свойства сильных оснований. В воде практически полностью диссоциируют, образуя щелочную среду и меняя окраску индикаторов.
Ba(OH)2 ↔ Ba2+ + 2OH—
Гидроксид магния — нерастворимое основание. Гидроксид бериллия проявляет амфотерные свойства.
10. Гидроксид и бериллия взаимодействует с щелочами. В расплаве образуются соли бериллаты, а в растворе щелочей — комплексные соли.
Например, гидроксид бериллия реагирует с расплавом гидроксида натрия:
Be(OH)2 + 2NaOH → Na2BeO2 + 2H2O
При взаимодействии гидроксида бериллия с избытком раствора щелочи образуется комплексная соль:
Be(OH)2 + 2NaOH → Na2[Be(OH)4]
Соли щелочноземельных металлов
Нитраты щелочноземельных металлов
Нитраты кальция, стронция и бария при нагревании разлагаются на нитриты и кислород. Исключение — нитрат магния. Он разлагается на оксид магния, оксид азота (IV) и кислород.
Например, нитрат кальция разлагается при нагревании на нитрит кальция и молекулярный кислород:
Ca(NO3)2 → Ca(NO2)2 + O2
Карбонаты щелочноземельных металлов
1. Карбонаты щелочноземельных металлов при нагревании разлагаются на оксид и воду.
Например, карбонат кальция разлагается при температуре 1200оС на оксид кальция и воду:
CaCO3 → CaO + CO2
2. Карбонаты щелочноземельных металлов под действием воды и углекислого газа превращаются в растворимые в воде гидрокарбонаты.
Например, карбонат кальция взаимодействует с углекислым газом и водой с образованием гидрокарбоната кальция:
CaCO3 + H2O + CO2 → Ca(HCO3)2
3. Карбонаты щелочноземельных металлов взаимодействуют с более сильными кислотами с образованием новой соли, углекислого газа и воды.
Более сильные кислоты вытесняют менее сильные из солей.
Например, карбонат магния взаимодействует с соляной кислотой:
CaCO3 + 2HCl → CaCl2 + CO2↑+ H2O
4. Менее летучие оксиды вытесняют углекислый газ из карбонатов при сплавлении. К менее летучим, чем углекислый газ, оксидам относятся твердые оксиды — оксид кремния (IV), оксиды амфотерных металлов.
Менее летучие оксиды вытесняют более летучие оксиды из солей при сплавлении.
Например, карбонат кальция взаимодействует с оксидом алюминия при сплавлении:
CaCO3 + Al2O3 → Ca(AlO2)2 + CO2↑
Жесткость воды
Постоянная и временная жесткость
Жесткость воды — это характеристика воды, обусловленная содержанием в ней растворенных солей щелочноземельных металлов, в основном кальция и магния (солей жесткости).
Временная (карбонатная) жесткость обусловлена присутствием гидрокарбонатов кальция Ca(HCO3)2 и магния Mg(HCO3)2 в воде.
Постоянная (некарбонатная) жесткость обусловлена присутствием солей, не выделяющихся при кипячении из раствора: хлоридов (CaCl2) и сульфатов (MgSO4) кальция и магния.
Способы устранения жесткости
Существуют химические и физические способы устранения жесткости. Химические способы устранения временной жесткости:
1. Кипячение. При кипячении гидрокарбонаты кальция и магния распадаются на нерастворимые карбонаты, углекислый газ и воду:
Ca(HCO3)2 → CaCO3 + CO2 + H2O
2. Добавление извести (гидроксида кальция). При добавлении щелочи растворимые гидрокарбонаты переходят в нерастворимые карбонаты:
Ca(HCO3)2 + Ca(OH)2 → CaCO3 + 2H2O
Химические способы устранения постоянной жесткости — реакции ионного обмена, которые позволяют осадить ионы кальция и магния из раствора:
1. Добавление соды (карбоната натрия). Карбонат натрия связывает ионы кальция и магния в нерастворимые карбонаты:
CaCl2 + Na2CO3 → CaCO3↓+ 2NaCl
2. Добавление фосфатов. Фосфаты также связывают ионы кальция и магния:
3CaCl2 + 2Na3PO4 → Ca3(PO4)2↓ + 6NaCl
Поделиться ссылкой:
chemege.ru
Щелочноземельные металлы | Дистанционные уроки
29-Авг-2012 | комментариев 15 | Лолита Окольнова
Давайте разберем эти металлы точно по подобию щелочных металлов.
Щелочноземельными эти металлы называют, т.к. они содержатся во всех минералах земли — поэтому «земельные», а «щелочные» — т.к. они придают воде щелочную реакцию.
Строение электронных оболочек
Электронное строение внешнего слоя у всех этих элементов одинаково – на нем всего 2 электрона на s-подуровне:
n S2
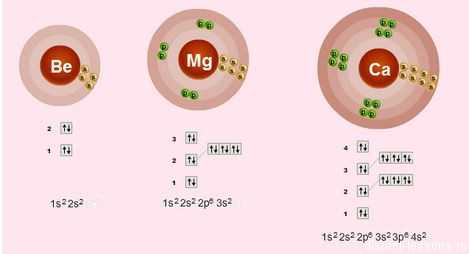
Что это означает?
- Валентности элементов = 2, т.е. каждый атом может образовывать 2 связи.
- Степень окисления элементов = +2 – металлические свойства – это способность отдавать электроны
- Сверху вниз в подгруппе радиус атома увеличивается, следовательно, электроны все слабее притягиваются к ядру атома, следовательно, сверху вниз металлические свойства увеличиваются – Ba более сильный металл, чем Be.
- Как следствие этого сверху вниз в подгруппе усиливаются восстановительные свойства.
Физические свойства щелочно-земельных металлов
Общие характеристики:
- все металлы сероватого цвета,
- твердые, ножом, как щелочные металлы, их уже, конечно, не порежешь 🙂
- плотность больше 1,
- на воздухе элементы достаточно устойчивы, но покрываются оксидной пленкой,
- окрашивают пламя в разный цвет (это используют для получения разных цветов пламени в пиротехнике):
Ca — в кирпично-красный
Sr – в красный
Ba– в желтый
- Электро- и теплопроводны
Химические свойства металлов
Имеет смысл рассмотреть химические свойства по таблице классификации неорганических соединений.
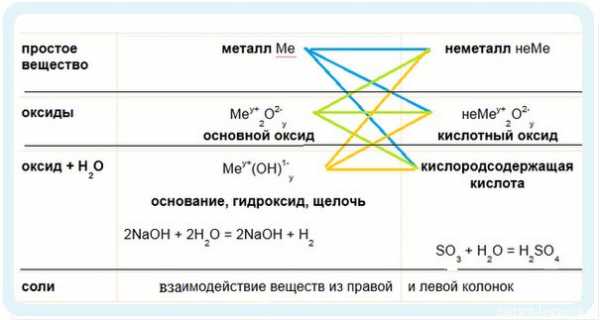
1. Идем по синим стрелочкам — взаимодействие металлов:
Металлы традиционно проявляют металлические — восстановительные свойства.
2. Идем по зеленым стрелочкам — реакции для оксидов
3. Идем по оранжевым стрелочкам
Обратите внимание, что гидроксиды щелочноземельных металлов либо малорастворимы, либо нерастворимые, поэтому их образование может служить качественной реакцией.
Be(OH)2 — амфотерный гидроксид, он может реагировать как с основаниями, так и с кислотами!
3. Щелочноземельные металлы с водородом также образуют гидриды.
Как мы уже говорили, сверху вниз в подгруппе металлические свойства элементов возрастают. Водород, хоть и находится в первой группе при реакции с щелочноземельными металлами будет проявлять отрицательную степень окисления.
Как определить качественные реакции? Загляните в таблицу растворимости!
Be(OH)2 — гелеобразный белый осадок;
Сa(OH)2 — белый осадок;
Mg(OH)2 — белесый осадок;
Фториды — белесо-бесцветные осадки;
Сульфиты и сульфаты — белые осадки.
Как видите, цвета осадков не отличаются цветовым разнообразием 🙂
Получение щелочно-земельных металлов
Обычно щелочноземельные металлы получают электролизом расплавов их солей:
CaCl2 (электролиз) → Ca + Cl2
Категории: |
Обсуждение: «Щелочноземельные металлы»
(Правила комментирования)distant-lessons.ru
общая характеристика, строение; свойства и получение — урок. Химия, 8–9 класс.
Щелочноземельными металлами называют \(4\) химических элемента \(I\)\(I\)\(A\) группы Периодической системы Д. И. Менделеева, начиная с кальция:
кальций \(Ca\), стронций \(Sr\), барий \(Ba\), радий \(Ra\).
Электронное строение атомов
На внешнем энергетическом уровне атомы металлов \(IIA\) группы имеют два электрона.
Поэтому для всех щелочноземельных металлов характерна степень окисления \(+2\).
Этим объясняется сходство их свойств.
Для металлов \(I\)\(I\)\(A\) группы (сверху вниз) характерно:
- увеличение радиуса атомов;
- уменьшение электроотрицательности;
- усиление восстановительных, металлических свойств.
Нахождение в природе
Из щелочноземельных металлов кальций наиболее широко распространён в природе, а радиоактивный радий — менее всего.
Все щелочноземельные металлы обладают высокой химической активностью, поэтому встречаются в природе только в виде соединений.
Основными источниками кальция являются его карбонаты CaCO3 (мел, мрамор, известняк).
В свободном виде простые вещества представляют собой типичные металлы от серого до серебристого цвета.
Физические свойства простых веществ
В твёрдом агрегатном состоянии атомы связаны металлической связью. Это обусловливает общие физические свойства простых веществ металлов: металлический блеск, ковкость, пластичность, высокую тепло- и электропроводность.
Тем не менее, металлы \(I\)\(I\)\(A\) группы имеют разные значения температуры плавления, плотности и других физических свойств.
Химические свойства
Щелочноземельные металлы обладают высокой химической активностью, реагируют с кислородом, водородом, другими неметаллами, оксидами, кислотами, солями.
Они являются сильными восстановителями.
Щелочноземельные металлы активно реагируют с:
водой, образуя соответствующие гидроксиды и выделяя водород:
Ba+2h3O=Ba(OH)2+h3↑;
кислотами, легко растворяясь в их растворах с образованием соответствующих солей:
Ba+2HCl=BaCl2+h3↑;
с неметаллами, образуя оксиды или соответствующие соли (гидриды, галогениды, сульфиды и др.):
Bа+Cl2=BаCl2,
Bа+S=BаS.
Щелочноземельные металлы получают в основном электролизом расплавов галогенидов. Чаще используются хлориды металлов.
При этом на катоде восстанавливаются катионы, а на аноде окисляются анионы.
Суммарное уравнение реакции электролиза расплава хлорида кальция:
CaCl2=Ca+Cl2↑.
www.yaklass.ru
