Что такое аммиак? Формула и свойства аммиака
Аммиак – соединение, являющееся важнейшим источником азота для живых организмов, а также нашедшее применение в различных отраслях промышленности. Что такое аммиак, каковы его свойства? Давайте разберемся.
Что такое аммиак: основные характеристики
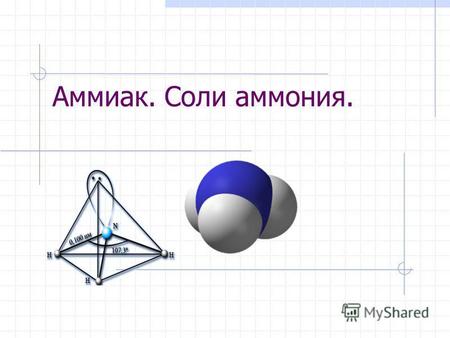
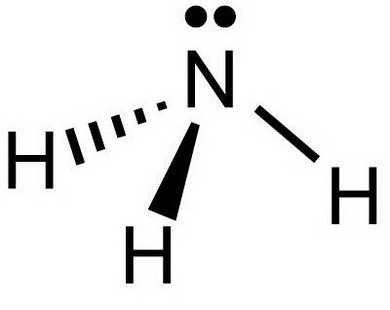
Аммиак (нитрид водовода) – соединение азота с водородом, имеющее химическую формулу NH3. Форма молекулы напоминает тригональную пирамиду, в вершине которой расположен атом азота.
Аммиак представляет собой газ, не имеющий цвета, но обладающий резким специфическим запахом. Плотность аммиака почти в два раза меньше, чем плотность воздуха. При температуре 15 oC она составляет 0,73 кг/м3. Плотность аммиака жидкого в нормальных условиях равна 686 кг/м3. Молекулярная масса вещества — 17,2 г/моль. Отличительной особенностью аммиака является его высокая растворимость в воде. Так, при температуре 0 °C ее значение достигает около 1200 объемов в объеме воды, при 20 °C – 700 объемов. Раствор «аммиак — вода» (аммиачная вода) характеризуется слабощелочной реакцией и довольно уникальным свойством по сравнению с другими щелочами: с увеличением концентрации плотность снижается.
Как образуется аммиак?
Что такое аммиак в организме человека? Это конечный продукт азотистого обмена. Большую его часть печень конвертирует в мочевину (карбамид) – менее токсичное вещество.
Аммиак в природных условиях образуется в результате разложения органических соединений, содержащих азот. Для использования в промышленности это вещество получают искусственным путем.
Получение аммиака в промышленных и лабораторных условиях
В промышленных условиях аммиак получают путем каталитического синтеза из азота и водорода:
N2 + 3H2 → 2Nh4 + Q.
Процесс получения вещества проводят при температуре 500 °C и давлении 350 атм. В качестве катализатора используется пористое железо. Полученный аммиак удаляется охлаждением. Азот и водород, которые не прореагировали, возвращаются на синтез.
В лабораторных условиях аммиак получают в основном путем слабого нагревания смеси, состоящей из хлорида аммония и гашеной извести:
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3↑ + 2H2O.
Для осушения готовое соединение пропускается через смесь извести и едкого натра. Довольно сухой аммиак можно получить путем растворения в нем металлического натрия и последующей перегонки.
Где используется аммиак?
Нитрид водорода широко применяется в различных отраслях промышленности. Огромные его количества используются для производства азотной кислоты и различных удобрений (мочевина, нитрат аммония и др.), полимеров, синильной кислоты, соды, аммониевых солей и других видов продукции химического производства.

В легкой промышленности свойства аммиака применяют при очистке и окрашивании таких тканей, как шелк, шерсть и хлопок. В сталелитейном производстве он используется для увеличения твердости стали путем насыщения ее поверхностных слоев азотом. В нефтехимической промышленности при помощи нитрида водорода нейтрализуют кислотные отходы.
Благодаря своим термодинамическим свойствам жидкий аммиак используется в качестве хладагента в холодильном оборудовании.
Раствор нитрида водорода (нашатырный спирт) применяется в медицине для выведения из обморочного состояния, стимуляции рвоты, для обработки рук медперсонала, при укусах насекомых и пр.

Некоторые химические свойства аммиака
Нитрид водорода характеризуется довольно высокой химической активностью и способен вступать в реакции со многими веществами.
При взаимодействии аммиака с кислотами образуются соответствующие соли аммония. Так, к примеру, в результате реакции с азотной кислотой образуется аммиачная селитра:
NH3 + HNO3 → NH4NO3.
При взаимодействии с HCl образуется хлорид аммония:
NH3+ HCl → NH4Cl.
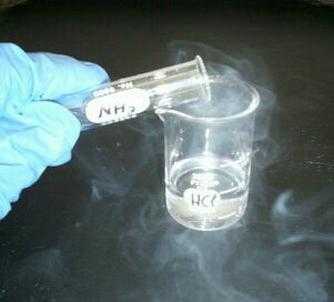
Соли аммония представляют собой твердые кристаллические вещества, разлагающиеся в воде и обладающие свойствами, присущими солям металлов. Растворы соединений, образованных в результате взаимодействия аммиака и сильных кислот, имеют слабокислую реакцию.
За счет атомов азота нитрид водорода является активным восстановителем. Восстановительные свойства его проявляются при нагревании. При горении в атмосфере кислорода он образует азот и воду. В присутствии катализаторов взаимодействие с кислородом дает оксид азота. Нитрид водорода имеет способность восстанавливать металлы из оксидов.
Галогены в результате реакции с аммиаком образуют галогениды азота – опасные взрывчатые вещества. При взаимодействии с карбоновыми кислотами и их производными нитрид водорода образует амиды. В реакциях с углем (при 1000 °С) и метаном он дает синильную кислоту.
С ионами металлов аммиак образует аминокомплексы, или аммиакаты (комплексные соединения), имеющие характерную особенность: атом азота всегда связан с тремя атомами водорода. В результате комплексообразования меняется окраска вещества. Так, к примеру, голубой раствор медного купороса при добавлении нитрида водорода приобретает интенсивный сине-фиолетовый цвет. Многие из аминокомплексов обладают достаточной устойчивостью. Благодаря этому они могут быть получены в твердом виде.

В жидком аммиаке хорошо растворяются как ионные, так и неполярные неорганические и органические соединения.
Санитарно-гигиенические характеристики
Аммиак относят к четвертому классу опасности. Предельно допустимая максимально-разовая концентрация (ПДК) в воздухе населенных пунктов равна 0,2 мг/м3, среднесуточная – 0,04. В воздухе рабочей зоны содержание аммиака не должно быть выше 20 мг/м³. При таких концентрациях запах вещества не ощущается. Фиксироваться человеческим обонянием он начинает при 37 мг/м³. То есть если запах аммиака ощущается, это означает, что допустимые нормы нахождения вещества в воздухе значительно превышены.
Влияние на человеческий организм
Что такое аммиак с точки зрения воздействия на человека? Это токсикант. Его относят к веществам, способным оказывать удушающее и нейротропное действие, ингаляционное отравление которыми может привести к отеку легких и поражению нервной системы.
Аммиачные пары раздражающе воздействуют на кожные покровы, слизистые оболочки глаз и органов дыхания. Концентрация вещества, при которой проявляется раздражение зева, составляет 280 мг на куб. метр, глаз − 490 мг на куб. метр. В зависимости количества нитрида водорода в воздухе могут возникать першение в горле, затрудненность дыхания, приступы кашля, боль в глазах, обильное слезотечение, химический ожог роговицы, потеря зрения. При содержании аммиака 1,5 г на куб. метр в течение часа развивается токсический отек легких. При контакте жидкого аммиака и его растворов (в высоких концентрациях) с кожей возможны покраснения, зуд, жжение, дерматиты. Так как сжиженный нитрид водовода при испарении поглощает тепло, возможны обморожения различной степени.
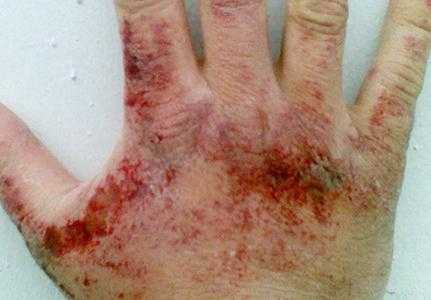
Симптомы отравления аммиаком
Отравление данным токсикантом может вызывать снижение слухового порога, тошноту, головокружение, головную боль и пр. Возможны изменения в поведении, в частности сильное возбуждение, бред. Проявление симптомов в ряде случаев имеет прерывистый характер. Они могут на некоторое время прекращаться, а потом возобновляться с новой силой.
Учитывая все возможные последствия воздействия аммиака, очень важно соблюдать меры предосторожности при работе с данным веществом и не допускать превышения его концентрации в воздушной среде.
fb.ru
Физические и химические свойства аммиака
Формула – NH3. Молярная масса – 17 г/моль.
Физические свойства аммиака
Аммиак (NH3) – бесцветный газ с резким запахом (запах «нашатырного спирта»), легче воздуха, хорошо растворим в воде (один объем воды растворят до 700 объемов аммиака). Концентрированный раствор аммиака содержит 25% (массовых) аммиака и имеет плотность 0,91 г/см3.
Связи между атомами в молекуле аммиака – ковалентные. Общий вид молекулы AB3. В гибридизацию вступают все валентные орбитали атома азота, следовательно, тип гибридизации молекулы аммиака – sp3. Аммиак имеет геометрическую структуру типа AB3E – тригональная пирамида (рис. 1).
Рис. 1. Строение молекулы аммиака.
Химические свойства аммиака
В химическом отношении аммиак довольно активен: он вступает в реакции взаимодействия со многими веществами. Степень окисления азота в аммиаке «-3» — минимальная, поэтому аммиак проявляет только восстановительные свойства.
При нагревании аммиака с галогенами, оксидами тяжелых металлов и кислородом образуется азот:
2NH3 + 3Br2 = N2 + 6HBr
2NH3 + 3CuO = 3Cu + N2 + 3H2O
4NH3 +3O2 = 2N2 + 6H2O
В присутствии катализатора аммиак способен окисляться до оксида азота (II):
4NH3 + 5O2 = 4NO + 6H2O (катализатор – платина)
В отличие от водородных соединений неметаллов VI и VII групп, аммиак не проявляет кислотные свойства. Однако, атомы водорода в его молекуле все же способны замещаться на атомы металлов. При полном замещении водорода металлом происходит образование соединений, называемых нитридами, которые также можно получить и при непосредственном взаимодействии азота с металлом при высокой температуре.
Основные свойства аммиака обусловлены наличием неподеленной пары электронов у атома азота. Раствор аммиака в воде имеет щелочную среду:
NH3 + H2O ↔ NH4OH ↔ NH4+ + OH—
При взаимодействии аммиака с кислотами образуются соли аммония, которые при нагревании разлагаются:
NH3 + HCl = NH4Cl
NH4Cl = NH3 + HCl (при нагревании)
Получение аммиака
Выделяют промышленные и лабораторные способы получения аммиака. В лаборатории аммиак получают действием щелочей на растворы солей аммония при нагревании:
NH4Cl + KOH = NH3↑ + KCl + H2O
NH4+ + OH
Эта реакция является качественной на ионы аммония.
Применение аммиака
Производство аммиака – один из важнейших технологических процессов во всем мире. Ежегодно в мире производят около 100 млн. т. аммиака. Выпуск аммиака осуществляют в жидком виде или в виде 25%-го водного раствора – аммиачной воды. Основные направления использования аммиака – производство азотной кислоты (производство азотсодержащих минеральных удобрений в последствии), солей аммония, мочевины, уротропина, синтетических волокон (нейлона и капрона). Аммиак применяют в качестве хладагента в промышленных холодильных установках, в качестве отбеливателя при очистке и крашении хлопка, шерсти и шелка.
Примеры решения задач
ru.solverbook.com
Получение аммиака в промышленности. Получение аммиака в лаборатории :: SYL.ru
На процесс производства оптимального количества химического вещества, а также достижения максимального его качества влияет ряд факторов. Получение аммиака зависит от показателей давления, температуры, наличия катализатора, используемых веществ и способа извлечения полученного материала. Эти параметры необходимо правильно сбалансировать для достижения наибольшей прибыли от производственного процесса.
Свойства аммиака
При комнатной температуре и нормальной влажности воздуха аммиак находится в газообразном состоянии и имеет очень отталкивающий запах. Он наделен ядовитым и раздражающим слизистые оболочки воздействием на организм. Получение и свойства аммиака зависят от участия в процессе воды, так как это вещество очень растворимо в нормальных характеристиках окружающей среды.
Аммиак является соединением водорода и азота. Его химическая формула – NH3.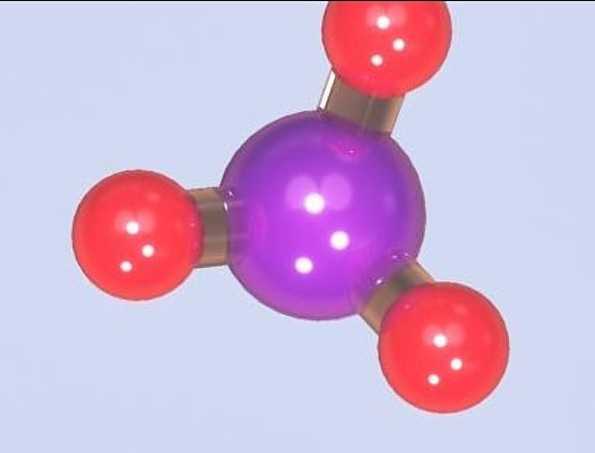
Это химическое вещество выступает активным восстановителем, в результате горения которого выделяется свободный азот. Аммиак проявляет характеристики оснований и щелочей.
Реакция вещества с водой
При растворении NH3 в воде получают аммиачную воду. Максимально при обычной температуре можно растворить в 1 объеме водного элемента 700 объемов аммиака. Известно это вещество как нашатырный спирт и широко применяется в отрасли производства удобрений, в технологических установках.
Полученный путем растворения в воде NH3 по своим качествам частично ионизирован.
Нашатырный спирт используется в одном из методов лабораторного получения этого элемента.
Получение вещества в лаборатории
Первый метод получения аммиака заключается в доведении нашатырного спирта до кипения, после чего полученный пар осушают и собирают требуемое химическое соединение. Получение аммиака в лаборатории возможно также путем нагревания гашеной извести и твердого хлорида аммония.
Реакция получения аммиака имеет такой вид:
2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 + 2H2O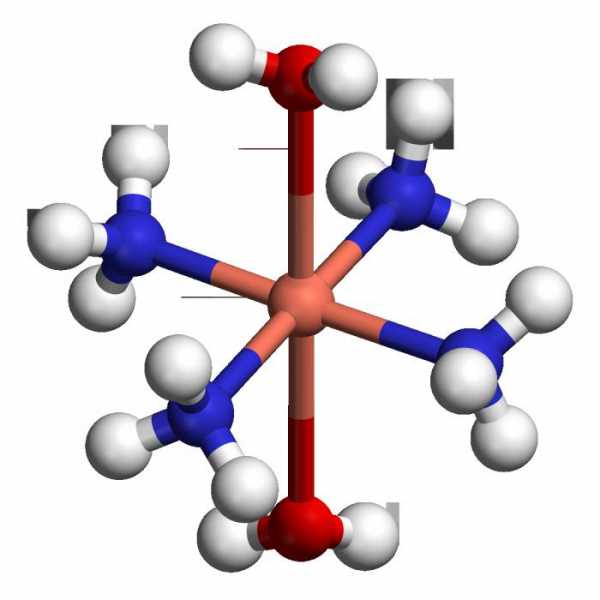
В ходе этой реакции выпадает осадок белого цвета. Это соль CaCl2, а еще образовывается вода и искомый аммиак. Для проведения осушения требуемого вещества его пропускают по смеси извести в сочетании с натром.
Получение аммиака в лаборатории не обеспечивает самую оптимальную технологию его производства в необходимых количествах. Люди много лет искали способы добычи вещества в промышленных масштабах.
Истоки налаживания технологий производства
На протяжении 1775-1780 годов были осуществлены опыты по связыванию свободных молекул азота из атмосферы. Шведский химик К. Шелле нашел реакцию, которая имела вид
Na2CO3 + 4C + N2 = 2NaCN + 3CO
На ее основе в 1895 году Н. Каро и А. Франк разработали метод связывания свободных молекул азота:
CaC2 + N2 = CaCN2 + C
Этот вариант требовал больших затрат энергии и был экономически невыгодным, поэтому со временем от него отказались.
Еще одним довольно затратным методом стал открытый английскими химиками Д. Пристли и Г. Кавендишем процесс взаимодействия молекул азота и кислорода:
N2 + O2 = 2NO
Рост потребности в аммиаке
В 1870 году это химическое вещество считалось нежелательным продуктом газовой промышленности и было практически бесполезным. Однако спустя 30 лет это оно стало очень востребованным в коксохимической отрасли.
Сначала возросшую потребность в аммиаке восполняли путем его выделения из каменного угля. Но при росте потребления вещества в 10 раз по поиску путей его добычи велась практическая работа. Получение аммиака стали внедрять с применением запасов атмосферного азота.
Потребность в веществах на основе азота наблюдалась практически во всех известных отраслях экономики.
Поиск путей удовлетворения промышленного спроса
Долгий путь прошло человечество к осуществлению уравнения производства вещества:
N2 + 3H2 = 2NH3
Получение аммиака в промышленности впервые удалось реализовать в 1913 году путем каталитического синтеза из водорода и азота. Способ открыт Ф. Габером в 1908 году.
Открытая технология разрешила давнюю проблему многих ученых разных стран. До этого момента не удавалось связать азот в виде NH3. Этот химический процесс получил название цианамидной реакции. При повышении температуры извести и углерода получалось вещество CaC2 (карбид кальция). Путем нагревания азота и добивались получения цианамида кальция CaCN2, из которого выделение аммиака проходило путем гидролиза.
Внедрение технологий для получения аммиака
Получение NH3 в глобальных масштабах промышленного потребления началось с покупки патента технологий Ф. Габера представителем Баденского содового завода А. Митташем. В начале 1911 года синтез аммиака на небольшой установке стал регулярным. К. Бош создал большой контактный аппарат, исходя из разработок Ф. Габера. Это было оригинальное оборудование, обеспечивающее процесс извлечения аммиака путем синтеза в производственном масштабе. К. Бош взял на себя все руководство по данному вопросу.
Экономия энергозатрат предполагала участие в реакциях синтеза определенных катализаторов.
Группа ученых, работающая над поиском подходящих составляющих, предложила следующее: железный катализатор, в который добавлялись оксиды калия и алюминия и который поныне считается одним из наилучших, обеспечивающих получение аммиака в промышленности.
9.09.1913 начал свою работу первый в мире завод, применяющий технологию каталитического синтеза. Постепенно наращивались производственные мощности, и к концу 1917 года вырабатывалось 7 тыс. т аммиака за месяц. В первый год работы завода этот показатель составлял всего 300 т в месяц.
Впоследствии во всех других странах тоже стали применять технологию синтеза с применением катализаторов, которая по своей сути не очень отличалась от техники Габера — Боша. Применение высокого давления и циркуляционных процессов происходило в любом технологическом процессе.
Внедрение синтеза в России
В России также применялся синтез с применением катализаторов, обеспечивающих получение аммиака. Реакция имеет такой вид:
N2 + 3H2 ↔ 2 NH3↑ + 45,9 кДж
В России самый первый завод аммиачного синтеза начал свою работу в 1928 году в Чернореченске, а далее были построены производства во многих других городах.
Практическая работа по получению аммиака постоянно набирает обороты. В период с 1960 по 1970 год синтез увеличился почти в 7 раз.
В стране для успешного получения, собирания и распознавания аммиака используют смешанные каталитические вещества. Изучение их состава осуществляет группа ученых под предводительством С. С. Лачинова. Именно эта группа нашла наиболее эффективные материалы для технологии осуществления синтеза.
Также постоянно ведутся исследования кинетики процесса. Научные разработки в этой области вели М. И. Темкин, а также его сотрудники. В 1938 году этот ученый вместе со своим коллегой В. М. Пыжевым сделал важное открытие, совершенствуя получение аммиака. Уравнение кинетики синтеза, составленное этими химиками, применяется отныне по всему миру.
Современный процесс синтеза
Процесс получения аммиака при помощи катализатора, применяемый в сегодняшнем производстве, имеет обратимый характер. Поэтому очень актуальным является вопрос оптимального уровня воздействия показателей на достижение максимального выхода продукции.
Процесс протекает при высокой температуре: 400-500 ˚С. Для обеспечения необходимой скорости прохождения реакции применяется катализатор. Современное получение NH3 предполагает использование высокого давления — около 100-300 атм.
Совместно с применением циркуляционной системы можно получить достаточно большую массу превращенных в аммиак первоначальных материалов.
Современное производство
Система работы любого аммиачного завода достаточно сложная и содержит в себе нескольких этапов. Технология получения искомого вещества осуществляется в 6 этапов. В процессе проведения синтеза происходит получение, собирание и распознавание аммиака.
Первоначальная стадия заключается в извлечении серы из природного газа при помощи десульфуратора. Эта манипуляция требуется вследствие того, что сера является каталитическим ядом и убивает никелевый катализатор еще на стадии извлечения водорода.
На втором этапе проходит конверсия метана, которая протекает с применением высокой температуры и давления при использовании никелевого катализатора.
На третьей стадии случается частичное выгорание водорода в кислороде воздуха. В результате производится смесь водяного пара, оксида углерода, а также азота.
На четвертом этапе происходит реакция сдвига, которая проходит при различных катализаторах и двух отличных температурных режимах. Первоначально применяется Fe3O4, и процесс протекает при температуре 400 ˚С. Во второй стадии участвует более эффективный по своему воздействию медный катализатор, что позволяет осуществление производства при низких температурах.
Следующая пятая стадия предполагает избавление от ненужного оксида углерода (VI) из смеси газа путем применения технологии поглощения раствором щелочи.
На завершающем этапе оксид углерода (II) удаляется при использовании реакции конверсии водорода в метан через никелевый катализатор и большую температуру.
Полученная в результате всех манипуляций смесь газа содержит 75 % водорода и 25 % азота. Ее сжимают под большим давлением, а затем остужают.
Именно эти манипуляции описывает формула выделения аммиака:
N2 + 3H2 ↔ 2 NH3↑ + 45,9 кДж
Хоть этот процесс выглядит не очень сложным, однако все вышеперечисленные действия по ее осуществлению говорят о сложности получения аммиака в промышленном масштабе.
На качество конечного продукта влияет отсутствие в сырье примесей.
Пройдя долгий путь от небольшого лабораторного опыта до масштабного производства, получение аммиака на сегодняшний день является востребованной и незаменимой отраслью химической промышленности. Этот процесс постоянно совершенствуется, обеспечивая качество, экономичность и необходимое количество продукта для каждой ячейки народного хозяйства.
www.syl.ru
Аммиак: свойства и все характеристики
Характеристики и физические свойства аммиака
Аммиак очень хорошо растворим в воде: 1 объем воды растворяет при комнатной температуре около 700 объемов аммиака. Концентрированный раствор содержит 25% NH 3 (масс.) и имеет плотность 0,91 г/см3. Раствор аммиака в воде иногда называют нашатырным спиртом. С повышением температуры растворимость аммиака уменьшается.
При низкой температуре из раствора аммиака может быть выделен кристаллогидрат NH3×H2O, плавящийся при -79oС. Известен также кристаллогидрат состава 2NH3×H2O.
Рис. 1. Строение молекулы аммиака.
Таблица 1. Физические свойства аммиака.
|
Молекулярная формула |
NH3 |
|
Молярная масса, г/моль |
17 |
|
Плотность, г/см3 |
0,6826 |
|
Температура плавления, oС |
195,42 |
|
Температура кипения, oС |
239,74 |
|
Растворимость в воде (0oС), г/100мл |
89,9 |
Получение аммиака
В лаборатории аммиак обычно получают6 нагревая хлорид аммония с гашеной известью:
2NH4Cl + Ca(OH)2 = CaCl2 + 2H2O + 2NH3↑.
Выделяющийся аммиак содержит пары воды. Для осушения его пропускают через натронную известь (смесь извести с едким натром).
Химические свойства аммиака
В химическом отношении аммиак довольно активен; он вступает во взаимодействие со многими веществами.
Если пропускать ток NH3 по трубке, вставленной в другую широкую трубку, по которой проходит кислород, то аммиак можно легко зажечь; он горит зеленоватым пламенем. При горении аммиака образуется вода и свободный азот:
4NH3 + 3O2 = 6H2O + 2N2.
При других условиях аммиак может окисляться до оксида азота NO.
При замещении в молекулах аммиака только одного атома водорода металлами образуются амиды металлов. Так, пропуская аммиак над расплавленным натрием, можно получить амид натрия NaNH2 в виде бесцветных кристаллов:
2Na + 3NH3 = 2NaNH2 + H2.
Аммиак реагирует с кислотами, находящимися в свободном состоянии или в растворе, нейтрализуя их и образуя соли аммония. Например, с соляной кислотой получается хлорид аммония NH4Cl:
NH3 + HCl = NH4Cl.
Взаимодействие аммиака с водой тоже приводит к образованию не только гидратов аммиака, но частично и иона аммония:
NH3 + H
Применение аммиака
Аммиак – одно из важнейших соединений азота: в больших количествах он расходуется в производстве азотных удобрений, взрывчатых веществ, полимеров, азотной кислоты и соды, используется в качестве холодильного агента в морозильных установках, а также в медицине.
Примеры решения задач
ru.solverbook.com
Раствор аммиака – получение и применение
Нитроген (азот) имеет несколько соединений с Гидрогеном (водород), из которых наиболее весомое значение имеет аммиак. В лабораторных условиях его получают при нагревании смеси хлорида аммония с гидроксидом калия. До конца 19 века чилийское месторождение натриевой селитры считали единственным источником соединений Нитрогена. Благодаря научным разработкам, химиками было предложено несколько методов фиксации атмосферного Нитрогена. Первым из них был цианамидный способ синтеза аммиака. Этот метод основан на свойстве азота соединяться с карбамидом кальция. Для этого пропускают азот через разогретый карбид кальция:
N2 + CaC2 = CaCN2 + С
Полученный таким образом CaCN2 (цианид кальция) используют в качестве нитратного удобрения в сельском хозяйстве. Следует сказать, что при обработке этого соединения водяным паром образуется аммиак:
CaCN2 + ЗН20 = 2Nh4+ СаС03
Аммиак перерабатывают на нитратную кислоту и азотные удобрения. В современной химии широко распространен другой метод получения Nh4 – синтез его из Нитрогена и Гидрогена:
1/2 N +3/2 h3 = Nh4
Полученный таким образом аммиак называют синтетическим. Промышленный синтез аммиака производят при наличии катализатора и при температуре 500 градусов.
Аммиак – газ, который имеет резкий характерный запах, он легче воздуха. Нельзя вдыхать Nh4 продолжительное время, поскольку он ядовит. Этот газ довольно хорошо растворяется в Н2О. Концентрированный водный раствор аммиака содержит 25 % Nh4.
При охлаждении (до -79°С) водный раствор аммиака переходит в кристаллогидрат. Научными исследованиями доказано, что основная масса Nh4 в водном растворе пребывает в виде гидратированных молекул (Nh4·nh3O) и лишь незначительная часть растворенного аммиака (около 0,5 %) взаимодействует с водой:
Nh4 + h3O = Nh5+ + ОН –
Щелочная реакция растворов аммиака обусловлена наличием гидроксид-ионов. Традиционно раствор аммиака обозначают как Nh5ОН. Щелочность раствора обуславливается наличием гидроксильной группы, которая образуется в результате диссоциации гидроксида аммония.
Раствор аммиака считают слабым основанием. В лабораториях иногда аммиак получают путем нагревания нашатыря. Аммиак довольно активное химическое соединение, взаимодействует со многими веществами, при этом проявляет только восстановительные свойства.
Аммиак горит, в присутствии Оксигена зеленовато-желтым пламенем, окисляясь при этом до свободного Нитрогена. При наличии катализатора (платины) окисление аммиака·идет дальше до образования оксида нитрогена. Эту реакцию используют в процессе получения нитратной кислоты. Следует сказать, что большая часть полученного таким образом аммиака расходуется на производство нитратных удобрений, а также нитратной кислоты.
В процессе испарения при -33,4 °С, жидкий Nh4 из окружающей среды поглощает очень много теплоты, вызывает охлаждение. Это свойство его используют в холодильных установках для получения искусственного льда при хранении скоропортящихся продуктов питания. Не редко жидкий аммиак используют при строительстве подземных конструкций. Раствор аммиака находит применение в лабораторной практике, химической промышленности, домашнем обиходе, и в медицине.
Раствор аммиака применение. Применяют как средство для возбуждения дыхания и выведения пациента из обморочного состояния. Большие концентрации Nh4 могут вызвать остановку дыхания. Иногда раствор аммиака используют как рвотное средство (10 капель на 100 мл воды). Следует учитывать, что это фармацевтическое средство нельзя применять наружно при наличии кожных заболеваний (экзема, дерматит). При отравлении парами аммиака медики назначают ацетатную, цитратную, тартратную (винную) кислоты в 1 % концентрации. В хирургической практике применяют раствор аммиака (25 мл/5 л кипяченой, теплой воды).
fb.ru
Получение аммиака в лабораторных и промышленных масштабах
Аммиак (Nh4) представляет собой химическое соединение водорода с азотом. Свое название он получил от греческого слова «hals ammniakos» или латинского «sal ammoniacus» которые переводятся одиноково — «нашатырь». Именно такое вещество под названием аммония хлорид получали в Ливийской пустыне в оазисе Аммониум.
Аммиак считается очень ядовитым веществом, которое способно раздражать слизистые оболочки глаз и дыхательных путей. Первичными симптомами отравления аммиаком являются обильное слезотечение, одышка и воспаление легких. Но вместе с тем, аммиак – ценное химическое вещество, которое широко используется для получения неорганических кислот, например, азотной, синильной, а также мочевины и азотсодержащих солей. Жидкий аммиак — это превосходное рабочее вещество холодильных контейнеров и машин, так как он имеет большую удельную теплоту испарения. Водные растворы аммиака используют как жидкие удобрения, а также для аммонизации суперфосфатов и туковых смесей.
Получение аммиака из отходящих газов в процессе коксования угля является древнейшим и весьма доступным методом, но на сегодняшний день он уже устарел и практически не используется.
Современным и основным способом является получение аммиака в промышленности на основе процесса Габера. Его суть в прямом взаимодействии азота и водорода, которое протекает в результате конверсии углеводородных газов. В качестве исходного сырья выступают обычно природный газ, газы нефтепереработки, попутные нефтяные газы, остаточные газы от производства ацетилена. Суть метода конверсионного получения аммиака состоит в разложении метана и его гомологов при высокой температуре на составляющие: водород и окись углерода с участием окислителей – кислорода и водяного пара. При этом к конвертируемому газу подмешивают воздух, обогащенный кислородом, либо атмосферный воздух. Изначально реакция получения аммиака на основе конвертируемого газа протекает с выделение тепла, но с понижением объема исходных продуктов реакции:
N2 + 3h3 ↔ 2Nh4 + 45,9 кДж
Однако получение аммиака в промышленных масштабах ведется с использованием катализатора и при искусственно созданных условиях, которые позволяют увеличить выход готового продукта. В атмосфере, где проходит получение аммиака, увеличивается давление до 350 атмосфер, а температура поднимается до 500 градусов Цельсия. При таких условиях выход аммиака — около 30%. Газ удаляется из зоны реакции с помощью метода охлаждения, а азот и водород, которые не прореагировали, возвращаются обратно в колонну синтеза и снова могут участвовать в реакциях. В ходе синтеза очень важно очистить смесь газов от каталитических ядов, веществ, способных сводить на нет действие катализаторов. Такими веществами являются пары воды, СО, As, P, Se, O2, S.
В качестве катализатора в реакциях синтеза азота и водорода выступает пористое железо с примесями оксидов алюминия и калия. Только это вещество, из всех 20 тысяч ранее перепробованных, позволяет достичь равновесного состояния реакции. Такой принцип получения аммиака считается самым экономичным.
Получение аммиака в лаборатории основано на технологии вытеснения его из аммониевых солей сильными щелочами. Схематически эта реакция представлена следующим образом:
2Nh5CI + Ca(OH)2 = 2Nh4 ↑+ CaCl2 + 2h3O
или
Nh5Cl + NaOH = Nh4↑ + NaCl + h3O
Чтобы удалить лишнюю влагу и осушить аммиак, его пропускают через смесь едкого натра и извести. Получение аммиака очень сухого достигается в результате растворения в нем металлического натра и последующей перегонки смеси. Чаще всего такие реакции проводят в закрытой металлической системе под вакуумом. Причем такая система должна выдержать высокое давление, которое достигается выделяющимися парами аммиака, до 10 атмосфер при комнатной температуре.
fb.ru
Получение аммиака | khimie.ru
Аммиак образуется при разложении азотсодержащих органических соединений. Поэтому в аммония он встречается также в природе, по большей части лишь в очень незначительных количествах. В отдельных местах земней поверхности, например, вблизи вулканов, такие соединения скапливаются в большом количестве. Однако для получения аммиака эти месторождения по существу, не имеют никакого значения. Важным источником получении аммиака является побочный продукт производства светильного газа кокса и сухой перегонки бурых углей − аммиачная вода (газовая вода, однако получаемое при этом количество аммиака не удовлетворяет потребности в нем. Поэтому огромное значение имеет получение аммиака непосредственно из атмосферного азота прямым каталитическим соединением азота с водородом по методу Габера-Боша.
Аммиак из газовой воды. Образующаяся главным образом при сухой перегонке каменных углей на газовых заводах и при коксовании углей газовая вода представляет собой бесцветную, пахнущую аммиаком, дегтем и сероводородом жидкость, которая содержит аммиак (большей частью 1-3 %) в виде различных солей, главным образом карбоната и, кроме того, в виде сульфида, сульфата, тиосульфата, хлорида, роданида и т. д. Аммиак из этого раствора сначала выделяют кипячением. При этом улетучивается, и та часть аммиака, которая находится в растворе в виде солей, так как они при кипячении гидролизуются; остаток аммиака отгоняют при добавлении к раствору известкового молока.
Из паров аммиака, смешанных с водяным паром и другими летучими веществами, сначала удаляют основные примеси, а именно С0
Иногда аммиак получают при перегонке с разложением отходов сахарного производства; в этом случае его получают главным образом в виде карбоната и сульфата аммония. В прежнее время аммиак и аммонийные соли получали из самих различных, содержащих азот отбросов органического происхождения, главным образом из перегнившей мочи. Нашатырь (хлорид аммония) этим способом приготовляли еще арабские алхимики. Одно время большое значении имел кальцийцианамидный способ приготовления аммиака Рота-Франка-Каро. Синтез аммиака этим способом основан на разложении кальцийцианамида при нагревании водяным паром или водой под давлением. В настоящее время по способу Рота-Франка-Каро кальцийцианамид производится еще в большом количестве, однако он используется почти исключительно в качестве удобрения, а не для производства аммиака.
Ваш отзыв
Вы должны войти, чтобы оставлять комментарии.
khimie.ru